RAS基因状态预测西妥昔单抗疗效研究撷萃
发布时间:[2014.01.24] 点击:196次
2014 Gastrointestinal Cancer Symposium (简称ASCO-GI)于2014年1月16-18日在美国旧金山顺利召开,来自世界各地近3000位胃肠肿瘤专家集聚一堂,围绕消化道肿瘤领域热点话题展开讨论。此次大会公布了三项KRAS/NRAS基因状态预测西妥昔单抗治疗mCRC疗效的研究。现总结如下:
研究一:KRAS和NRAS突变对西妥昔单抗加FOLFOX4一线治疗转移性结直肠癌(mCRC)患者的治疗结局的影响:来自OPUS研究的新结果。
研究背景
在一线FOLFOX4方案基础上添加西妥昔单抗,可明显改善KRAS基因外显子2、密码子12/13野生型(wt)的mCRC患者的应答和无进展生存。
研究方法
对于之前在OPUS研究中确定为KRAS密码子12/13野生型的患者(179 例),利用BEAMing技术对其肿瘤进行KRAS基因外显子3和4 (8个)和NRAS外显子2 、3和4(18个)的特定基因突变筛查。
研究结果
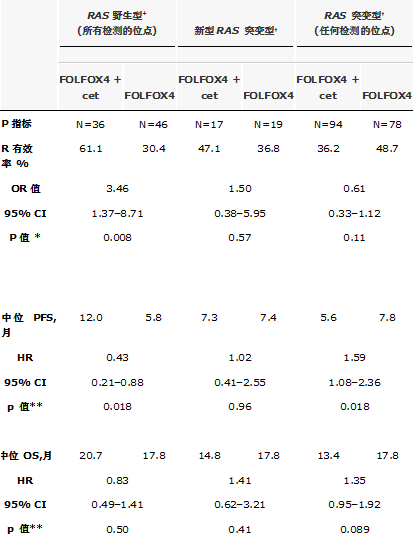
179 例中的118例(66%) 患者可进行RAS突变状态评价。36例(31 %)患者检测到这些位点的突变。RAS野生型人群可从西妥昔单抗添加到FOLFOX4方案中获益(表)。而RAS突变人群的临床结局则相对不太好,未能从西妥昔单抗的添加中获益。
结论
具有KRAS或NRAS突变的mCRC患者,不太可能从FOLFOX4方案添加西妥昔单抗中获益。由于患者数量较少,不能对新发的肿瘤基因突变患者下明确结论。限定在这些基因位点野生型的肿瘤患者身上使用西妥昔单抗可能有助于制定进一步的个性化治疗,从而使患者的受益最大化。
来源:J Clin Oncol 32, 2014(suppl 3; abstrLBA444)
研究二:FOLFOX4加每周或每2周一次的西妥昔单抗一线治疗KRAS和NRAS野生型(wt)转移性结直肠癌(mCRC)
研究背景
随机II期CECOG/CORE2研究报告称,对于152例KRAS基因外显子2 野生型mCRC患者,一线FOLFOX4联合两种方式的西妥昔单抗(每周或每两周一次)的疗效和安全性相似。最近的分析还表明,KRAS基因外显子3/4和NRAS (外显子2 、3和4)突变也与EGFR靶向单克隆抗体治疗后较差的PFS和OS有关。研究人员就这些突变对CECOG/CORE2研究中报告结果的影响进行了研究。
研究方法
通过常规Sanger测序对148例随机分配的KRAS基因外显子2野生型mCRC患者的肿瘤样品进行了额外的突变检测。对KRAS(外显子2 ,3和4)和NRAS(外显子2 ,3和4)野生型肿瘤患者[RAS wt]与KRAS(外显子3和4)或NRAS(外显子2 ,3和4)突变患者[RAS mt]的客观缓解率(ORR),PFS和OS进行比较。比较中排除BRAF突变。使用科克伦-曼特尔-亨塞尔法比较ORR 。采用Kaplan-Meier法,log-rank检验和Cox比例风险方法分析PFS和OS。
研究结果
148例 KRAS基因外显子2野生型患者中,124例为RAS和BRAF 野生型,10例仅有RAS基因突变,14例仅有BRAF突变。RAS野生组及RAS 突变组的ORR分别为61.3 % ( 95%CI , 52.1-69.9 )和40 % (95%CI ,12.2-73.8 ),(OR 0.43,P = 0.1966 ) 。中位PFS分别为为9.7个月( 95 % CI, 8.9-11.2 )及7.2个月(95 % CI, 6.7-10.8 ),( HR = 0.56 ,P = 0.1135 )。中位OS分别为28.5个月(95 %CI ,24.0-31.3 )及16.3个月(95%CI ,15.9-20.7 ),( HR = 0.43 ,P = 0.0199 )。如果调整明显的混杂因素,Cox模型显示OS差异具有统计学意义。BRAF 突变和RAS 突变患者的ORR ,PFS和OS相似。
结论
与 RAS 突变患者相比,采用西妥昔单抗与FOLFOX4治疗的 RAS 野生型患者的OS明显延长。这项分析支持其它试验的发现:EGFR靶向单克隆抗体治疗开始前建议进行mCRC疾病的RAS突变分析。
来源:J Clin Oncol 32, 2014(suppl 3; abstrLBA391)
研究三:EGFR信号通路突变:对FIRE-3研究中疗效的影响
研究背景
FIRE-3研究( AIO KRK - 0306 )为一项随机多中心试验,比较FOLFIRI方案加西妥昔单抗(cet)与FOLFIRI方案加贝伐单抗(bev)一线治疗KRAS野生型mCRC患者的疗效。与FOLFIRI加bev相比,FOLFIRI加cet一线治疗KRAS野生型mCRC患者的总体缓解率(ORR)和无进展生存期(PFS)无明显差异 ,FOLFIRI加cet组的总生存期(OS)明显较长。
研究方法
在一项预先计划的分析中,对EGFR途径中突变的影响进行了调查。对KRAS(外显子2,3 ,4), NRAS (外显子2,3,4)和BRAF (V600E)突变 ,以及PIK3CA突变(外显子9和20)和Akt突变进行了研究,并评估了其对FIRE-3研究人群的ORR,PFS,OS的影响。采用焦磷酸测序对所有突变进行了分析。
研究结果
ITT人群包括592例 KRAS野生型(外显子2)患者,当前分析获得了488例(82.4%)肿瘤组织样本。对407例患者进行了所有RAS基因突变测序。FOLFIRI加cet治疗后RAS野生型患者组的ORR较高( 65.5 % vs 59.6 % ; Fisher's p值= 0.157 )。对于RAS野生型患者的HRs(cet;bev),PFS及OS分别为0.93( 95%CI 0.74-1.17 ,P = 0.54)及0.70( 95%CI为0.53-0.92 ,P = 0.01)。与采用bev加FOLFIRI 治疗的RAS野生型患者相比,PIK3CA突变不影响PFS及OS。
结论
对于无RAS突变的患者,与bev联合 FOLFIRI治疗相比,cet联合FOLFIRI方案治疗使患者的 ORR和OS显著升高。排除RAS突变患者确定了更可能从西妥昔单抗中获益的人群。
来源:J Clin Oncol 32, 2014(suppl 3; abstrLBA445)
专家点评 北京大学肿瘤医院 李健教授
在2013年PRIME研究公布新的RAS基因检测可进一步预测抗EGFR单抗疗效后,mCRC抗EGFR单抗治疗寻找到了进一步的疗效预测因子,向个体化治疗又迈进了一步;但PRIME研究仅证实了新RAS基因突变无法从帕尼单抗联合FOLFOX治疗中获益,RAS基因状态能否预测帕尼单抗与西妥昔单抗联合FOLFIRI疗效尚缺乏足够证据,本次会议中Abstract LBA387研究与OPUS研究初步结果显示了新RAS基因突变无法从西妥昔单抗联合FOLFOX一线治疗、帕尼单抗联合FOLFIRI二线治疗中获益,而最后一块拼图新RAS突变能否预测西妥昔单抗联合FOIFIRI疗效我们期待CRYSTAL研究的后续结果来回答。
2013年我们更多地谈论了KRAS-BRAF-NRAS-PI3K等一系列基因筛查后,mCRC患者接受抗EGFR单抗治疗获益逐步增多,但这中间BRAF仅是预后因素,而非明确的疗效预测因子,PI3K的预测作用亦尚未得到最终明确,因此,在RAS基因突变状态逐渐被明确为抗EGFR单抗疗效预测因子后,其它因子的预测价值仍有待于进一步确认。
此外,结直肠癌中新的RAS基因的被发掘,启示我们在其它实体瘤的常规基因检测之外,是否也应逐步重视少见的突变类型对个体化治疗的作用。
来源:医脉通综合