十二指肠灌注生大黄对SD大鼠胰腺外分泌的影响
发布时间:[2011.06.27] 点击:156次
摘要
目的: 观察十二指肠灌注生大黄对SD大鼠胰腺外分泌的影响.
方法: 取体质量250-300 g SD大鼠24只, 随机分为2组(n = 12). 麻醉后在大鼠幽门下5 mm和十二指肠、空肠交界处分别置直径2 mm的塑料管并固定; 从十二指肠乳头Oddi括约肌处留置直径0.7 mm的塑料留置管. 稳定30 min后,每隔15 min收集1次胆胰混合液, 测定体积后留取100 μL胆胰混合液用双蒸水稀释以测定蛋白质含量, 剩余的胆胰混合液在下一收集时间内灌入十二指肠. 收集5管基础状态胆胰混合液后实验组以3 mL/h的速度向十二指肠内灌注生大黄2 h, 并收集8管胆胰混合液进行体积和蛋白质测定. 对照组不进行十二指肠灌注.
结果: 十二指肠灌注生大黄后胆胰混合液体积较基础状态增加30.95%, 与对照组比较, 差别有统计学意义(P <0.01); 蛋白质分泌量较基础状态增加5.02%, 但与对照组比较, 其差别无统计学意义(P >0.05).
结论: 对大鼠进行十二指肠灌注生大黄后单位时间内胆胰混合液分泌的体积增加, 但蛋白质分泌量无明显增加.
引言
餐后胰腺外分泌是食物消化吸收过程中的重要组成部分, 在蛋白质、脂肪和碳水化合物的消化中起着重要的作用. 胰液外分泌分为头期、胃期、肠期, 其中以肠期最为重要. 生大黄作为重症急性胰腺炎(severe acute pancreatitis, SAP)综合治疗的重要组成部分, 已得到学者的充分肯定, 但其具体作用机制尚不明确[1-6]. 本研究采用外分泌功能研究大鼠模型直接收集大鼠胆胰混合液测定胆胰混合液的体积、蛋白质含量,观察十二指肠灌注生大黄对胰腺外分泌功能的影响.
1 材料和方法
1.1 材料 健康的SD大鼠24只, ♂, 由温州医学院实验动物中心提供. 直径0.7 mm的一次性使用intima-Ⅱ静脉留置针购于江苏碧迪医疗器械有限公司. BCA试剂盒为PIERCE公司产品.
1.2 方法
1.2.1 分组及大鼠处理: 健康♂SD大鼠24只, 清洁级, 体质量250-300 g, 随机分为2组, 对照组(假手术组)12只, 实验组(生大黄煎液组)12只. 实验前大鼠禁食过夜, 自由饮水. 以2%氯胺酮腹腔麻醉(60-80 mg/kg), 建立外分泌功能研究大鼠模型[7], 在大鼠幽门下5 mm和十二指肠、空肠交界处分别置直径2 mm的塑料管并固定; 从十二指肠乳头Oddi括约肌处留置直径0.7 mm的塑料留置管. 通过红外线烤灯使大鼠肛温维持在37 ℃左右, 实验过程中每30 min追加1次1/3麻醉剂量的氯氨酮. 动物稳定30 min后, 每隔15 min收集一次胆胰混合液, 测定体积后留取100 mL胆胰混合液用双蒸水稀释以测定蛋白含量, 其余部分胆胰混合液在下一收集时段内从幽门下留置管内匀速注入十二指肠. 收集5管基础状态胆胰混合液后开始以微量注射泵按3 mL/h的速度向十二指肠内灌注0.5 g/mL生大黄煎液2 h, 并收集8管灌注后胆胰混合液. 对照组除了不进行十二指肠灌注外, 其余处理同实验组.
1.2.2 胆胰混合液体积测定: 采用微量进样器测定胆胰混合液体积(mL).
1.2.3 胆胰混合液蛋白测定: 采用BCA法. 操作流程严格按照BCA蛋白质检测试剂盒说明书进行.
统计学处理 数据以mean±SD表示, 采用SPSS16.0统计分析软件分析, 采用t 检验对各组均数进行显著性检验, P <0.05为差异具有统计学意义.
2 结果
2.1 十二指肠灌注生大黄对大鼠单位时间内胆胰混合液分泌体积的影响 对照组180 min内单位时间(15 min)分泌的胆胰混合液体积无明显变化, 实验组十二指肠内灌注生大黄2 h后单位时间分泌的胆胰混合液体积均值较注射前增加30.95%(P <0.01). 对照组和实验组在后120 min内胆胰混合液的蛋白分泌量各时间点均值比较,在105、120、150、165、180 min有显著性差别(P <0.05, 图1).
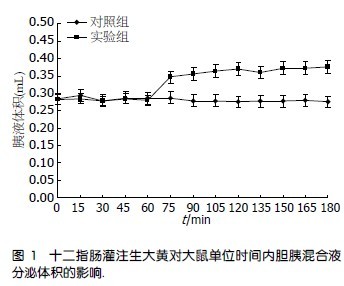
2.2 十二指肠灌注生大黄对大鼠单位时间内胆胰混合液蛋白分泌量的影响 单位时间的胆胰混合液蛋白分泌量根据单位时间内分泌的胆胰混合液体积乘以同时间段内胆胰混合液的蛋白含量计算, 以15 min为一个单位. 实验组十二指肠内灌注生大黄后, 胆胰混合液蛋白分泌量均值较注射前增加5.02%(P >0.05). 对照组和实验组在后120 min内胆胰混合液的蛋白分泌量各时间点均值比较, 胆胰混合液蛋白分泌量无明显差异(P >0.05, 图2).
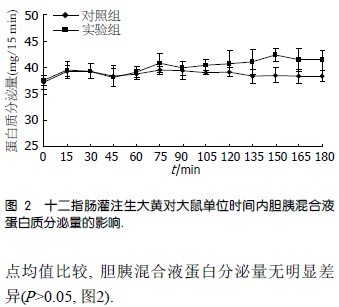
3 讨论
急性胰腺炎(acute pancreatitis, AP)是临床常见的急腹症之一, 胰酶对胰腺组织的自身消化是导致AP发病的重要因素, 是指多种病因引起的胰酶激活, 继以胰腺局部炎症反应为主要特征, 伴或不伴有其他器官功能改变的疾病. 分为轻型急性胰腺炎(mild acute pancreatitis, MAP)和SAP,后者病死率达10%[8].
中医用于治疗胰腺炎的方剂如大承气汤、大陷胸汤、柴芩承气汤、柴芍承气汤、清胰汤、清胰解毒汤, 基本都含有大黄. 中医将大黄对AP的治疗功用归之为通里攻下、清热利胆、活血化瘀. 运用大黄等中药用于治疗SAP已成为是我国独有的SAP综合治疗的一重要组成部分.
学者研究发现, 生大黄抑制胰酶活性, 抑制巨噬细胞过度澈活及中性粒细胞浸润, 减少炎症细胞因子及自由基的释放, 还抑制血管通透性, 松弛Oddi括约肌, 促进胃肠道蠕动, 维护肠管屏障功能, 免除肠菌易位, 可有效改善大鼠急性出血性胰腺炎的严重程度[9-11]. 但对于肠内给予生大黄对胰腺外分泌功能的直接影响很少有人研究.
因大鼠胰液的收集比较困难, 根据文献报道, 非CCK刺激引起的蛋白分泌属胰源性, 并不引起胆汁中蛋白含量的增加, 因此收集胆胰混合液测定蛋白质含量可以很好地反映胰液蛋白质含量的变化, 同时由于未结扎胆管, 使大鼠更趋于生理状态, 结果更可靠[12,13]. 本研究采用外分泌功能研究大鼠模型直接收集大鼠胆胰混合液测定胆胰混合液的体积、蛋白质含量以直观反映胰腺外分泌功能, 观察十二指肠灌注生大黄对胰腺外分泌功能的影响. 结果发现十二指肠灌注生大黄后胆胰混合液体积较基础状态增加, 但蛋白质分泌量无明显增加, 即胰酶分泌无明显增加. 因此我们认为, 在AP患者早期胃管内注入生大黄煎剂, 不会增加胰酶的分泌, 且生大黄价格低廉, 使用方便, 无明显不良反应, 可作为辅助治疗SAP的理想药物.
4 参考文献
[1]周黎明, 万莉红, 李贵星, 王正荣. 大黄素对大鼠急性坏死型胰腺炎的干预作用. 中药药理与临床 2006; 22:15-16。
[2] 幸军, 冯青青, 李春安, 樊拖迎. 善得定和生大黄联合应用治疗重症急性胰腺炎. 中华急诊医学杂志 2004;13: 468-469。
[3] 袁楚明, 陈梦云, 李奕琏, 陈健芳. 早期应用生大黄对重症急性胰腺炎的疗效. 胰腺病学 2007; 7: 31-33。
[4] 王刚, 孙备, 孟庆辉, 姜洪池. 早期肠内营养联合生大黄对大鼠急性坏死性胰腺炎肝损伤的影响. 胰腺病学2007; 7: 104-106。
[5] 姚圣华, 朱阳春, 李淑德. 清胰汤及生大黄灌肠治疗重症急性胰腺炎最佳应用时间探讨. 中华胰腺病杂志2008; 8: 324-325。
[6] 盛颖玥, 邹晓平, 于成功, 吕瑛, 张丽莉. 中药大黄辅助治疗重症急性胰腺炎的系统评价. 世界华人消化杂志2010; 18: 730-735。
[7] 陈小燕, 李兆申, 屠振兴, 曹晓鹏. 胰腺外分泌功能研究大鼠模型的建立. 世界华人消化杂志 2005; 13:1760-1762。
[8] Andersen AM, Novovic S, Ersb?ll AK, Hansen MB.Mortality in alcohol and biliary acute pancreatitis.Pancreas 2008; 36: 432-434。
[9] 巫协宁. 重症胰腺炎的规范化治疗和治疗策略. 中华消化杂志 2001; 21: 300-302。
[10] 刘晓红, 赵雩卿, 钱家鸣. 大黄对大鼠急性出血性胰腺炎的影响. 中华消化杂志 2004; 24: 14-17。
[11] 王刚, 孙备, 姜洪池, 许军. 早期肠内营养联合大黄治疗重症急性胰腺炎的实验研究. 中华普通外科杂志2006; 21: 150。
[12] Zhu JX, Zhu XY, Owyang C, Li Y. Intestinalserotonin acts as a paracrine substance to mediatevagal signal transmission evoked by luminal factorsin the rat. J Physiol 2001; 530: 431-442。
[13] 夏青, 李兆申, 屠振兴, 龚燕芳, 满晓华. 大鼠孤束核在五羟色胺介导的胰腺外分泌中的作用. 世界华人消化杂志 2004; 12: 2805-2808。来源:华语消化网